Nos equivocamos: Pensamos que sólo era un virus respiratorio
Por Ariel Bleicher and Katherine Conrad. UCSF Magazine. Verano 2020
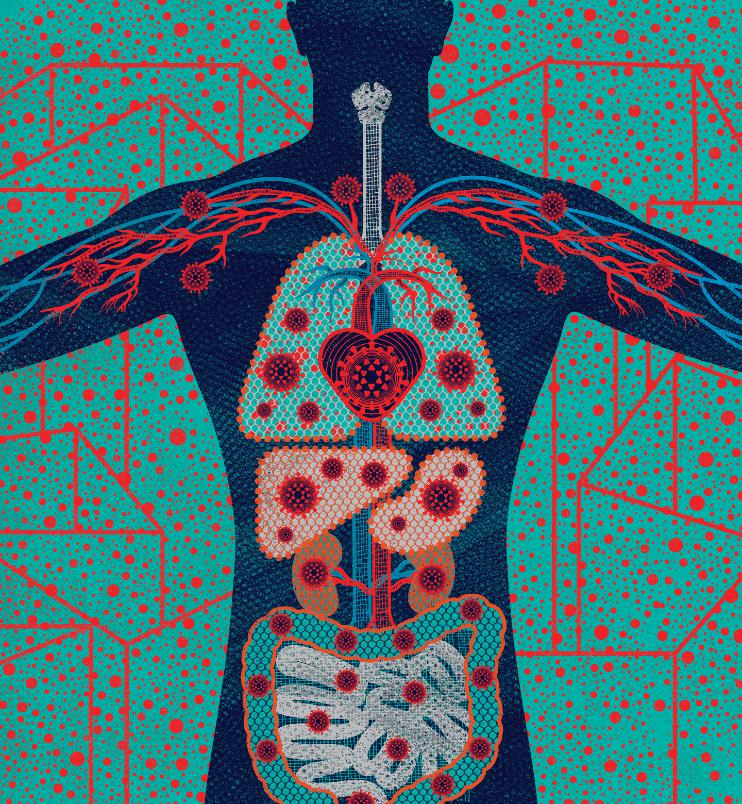
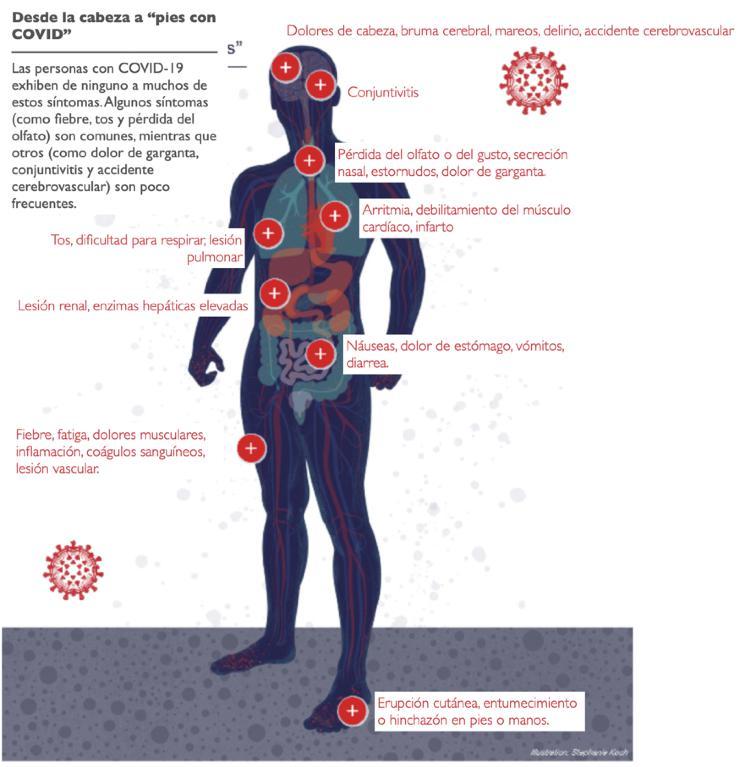
A fines de enero, cuando los hospitales de los Estados Unidos confirmaron la presencia del nuevo coronavirus, los trabajadores de la salud sabían que debían estar al pendiente de vigilar tres síntomas precisos: fiebre, tos y falta de aire. Pero a medida que aumentó la cantidad de infecciones, la lista de síntomas comenzó a crecer. Algunos pacientes perdieron el sentido del olfato y el gusto. Algunos tenían náuseas o diarrea. Algunos tenían arritmias o incluso ataques al corazón. Algunos tenían riñones o hígados dañados. Algunos tenían dolores de cabeza, coágulos de sangre, erupciones cutáneas, hinchazón o derrames cerebrales. Muchos no tenían síntomas en absoluto.
Para junio, los médicos intercambiaban artículos de revistas, noticias y tuits que describían más de tres docenas de formas en que el COVID-19, la enfermedad que causa el coronavirus, parece manifestarse. Ahora los investigadores de la Universidad de California en San Francisco y de todo el mundo han comenzado a analizar más de cerca esta vertiginosa variedad de síntomas para descubrir las causas de la enfermedad. Están aprendiendo de personas dentro y fuera del hospital; personas al borde de la muerte y sólo levemente enfermas; personas recién expuestas y recuperadas; personas jóvenes y viejas, negras, morenas y blancas. Y están empezando a reconstruir la historia de un virus como ningún otro conocido antes.
Cómo se asienta la infección
Los virus llevan una curiosa existencia transitoria de no estar ni completamente vivos ni muertos. Envuelto en una capa de proteína, un virus consiste casi por completo en material genético: ADN o ARN, los modelos para todo tipo de vida. Pero no puede reproducirse por sí solo. Para sobrevivir, debe penetrar en una célula y apropiarse la maquinaria de copia de genes de la célula.
El nuevo coronavirus, un virus de ARN llamado SARS-CoV-2, se ha hecho famoso por su habilidad para romper y entrar a las células humanas. Sus herramientas favoritas son los picos de proteínas que sobresalen de su superficie, una característica que distingue a todos los coronavirus. Los picos del SARS-CoV-2 son la crème de la crème: por la fortuna que les confirió el sorteo evolutivo, son capaces de agarrarse fácilmente a las compuertas de las proteínas en las células humanas conocidas como receptores ACE2 y, al igual que las ganzúas, abrir estas compuertas.

“Se puede pensar en un receptor ACE2 como un sitio de acoplamiento”, dice Faranak Fattahi, PhD, miembro de la UCSF Sandler. Cuando la pandemia de coronavirus golpeó a San Francisco, Fattahi reacondicionó su laboratorio para estudiar este receptor clave, que normalmente juega un papel en la regulación de la presión arterial. “Cuando el virus cae sobre él”, dice, “inicia un proceso molecular que lleva el virus al interior de la célula”.
Si eres expuesto al SARS-CoV-2, —por ejemplo, por toser o estornudar—, es probable que el virus primero encuentrereceptores ACE2 en las células de la nariz o la garganta. Pero estos receptores también pueblan tu corazón, intestino y otros órganos. El equipo de Fattahi ha encontrado evidencia que sugiere que las hormonas sexuales masculinas como la testosterona pueden aumentar la cantidad de receptores ACE2 que producen las células, lo que podría ayudar a explicar por qué el SARS-CoV-2 parece causar más estragos en los hombres que en las mujeres y por qué los niños rara vez se enferman. “Cuantos menos receptores ACE2, menos riesgo de infección, esa es la idea”, dice, y agrega que esta hipótesis de la brecha de género de la enfermedad es sólo una de varias.
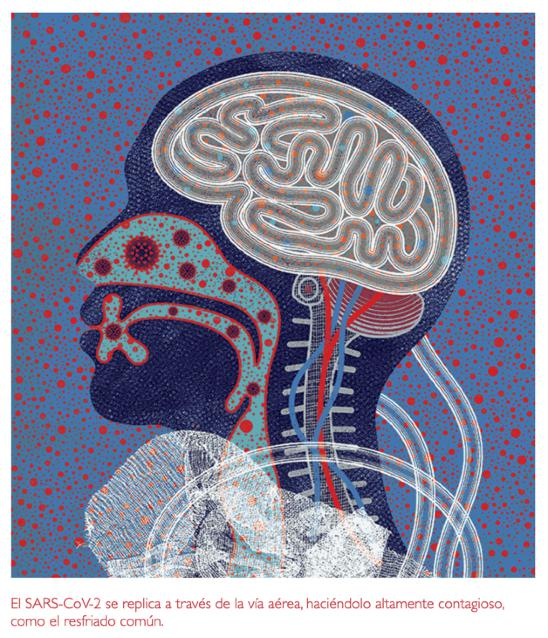
Una vez dentro de unas pocas células huésped iniciales, el virus las pone a trabajar produciendo copias de sí mismo. En cuestión de horas, miles de nuevas partículas de virus comienzan a estallar, listas para infectar más células. Aunque el SARS-CoV-2 es menos mortal que el virus del SARS original, que surgió en 2002, se replica más rápidamente. Además, a diferencia del SARS, que infecta principalmente los pulmones, el SARS-CoV-2 se replica en toda la vía aérea, incluida la nariz y la garganta, lo que lo hace muy contagioso, como el resfriado común.
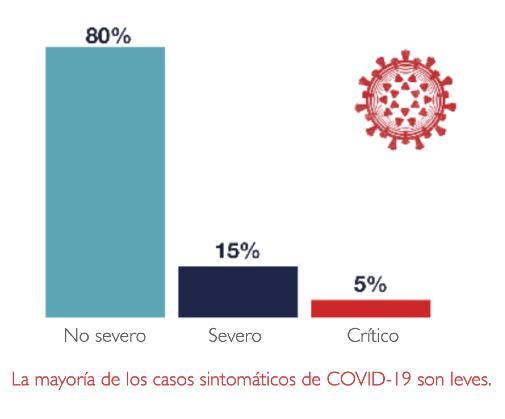
Sin embargo, la infección con SARS-CoV-2 generalmente no se siente como un resfriado. Menos del 20% de las personas infectadas que finalmente aparecen en un hospital informan haber tenido dolor de garganta o secreción nasal. Durante los primeros días de la infección, es más probable que tenga fiebre, tos seca o, en particular, que pierda el sentido del olfato o el gusto.
Sin embargo, lo más probable es que la persona no se sienta enferma en absoluto. Cuando los investigadores de UCSF evaluaron a personas con SARS-CoV-2 de Mission District en San Francisco, el 53% de las personas infectadas nunca tuvieron síntomas. “Eso es mucho más alto de lo esperado”, dice Monica Gandhi, MD, MPH, profesora de medicina de la UCSF con experiencia en VIH. Las encuestas de brotes en hogares de ancianos y prisiones muestran números similares o incluso mayores.
“Si hiciéramos una campaña de pruebas masivas en 300 millones de estadounidenses en este momento, creo que la tasa de infección asintomática estaría entre el 50% y el 80% de los casos”, dice Gandhi. Millones de personas pueden estar propagando el virus sin saberlo, señala, haciendo de la transmisión asintomática el talón de Aquiles para controlar la pandemia, y destacando la importancia del uso generalizado del cubrebocas.
“La mayoría de las personas que tienen COVID-19 están en la comunidad y son asintomáticas o sólo están levemente enfermas”, dice Sulggi Lee, MD, PhD, profesora asistente de medicina de la UCSF. Cuando la pandemia de coronavirus golpeó a San Francisco a principios de marzo, Lee concibió un estudio para investigar por qué. Se apresuró a reunir un equipo y obtener fondos y equipamiento. Tomó prestada la clínica móvil de un colega, una camioneta equipada con una mesa de examen y una silla de flebotomía, para que su equipo pudiera conducir por la ciudad, recolectando muestras de personas infectadas. Lee espera que los datos del estudio, llamado CHIRP (COVID-19 Host Immune Response Pathogenesis), muestren cómo responden los sistemas inmunes de las personas a medida que el SARS-CoV-2 comienza a establecerse en sus cuerpos.
“Mucho depende de esa respuesta inicial”, dice ella. Si Lee y sus colaboradores pueden descubrir los procesos biológicos que permiten que algunas personas infectadas se mantengan relativamente bien, tal vez puedan usar ese conocimiento para evitar que otros caigan gravemente enfermos.
Luchando en los pulmones
Fiel a su nombre, el SARS-CoV-2 (que significa coronavirus tipo 2 del síndrome respiratorio agudo grave) es, ante todo, un virus respiratorio malo. Si tu sistema inmunológico no lo vence en su sitio de aterrizaje en la nariz o la garganta, avanzará por la tráquea, infiltrándose en las células que recubren los tubos de aire ramificados de los pulmones. En los extremos de los tubos, pequeños sacos de aire llamados alvéolos pasan oxígeno a la sangre. A medida que el virus se multiplica, los alvéolos pueden llenarse de líquido, interrumpiendo este intercambio crítico de gases. Tu nivel de oxígeno en la sangre puede disminuir y, por lo general, aproximadamente seis días después de una infección, puedes comenzar a sentir dificultad para respirar.
¿Qué causa este caos? “Parte de esto es definitivamente causado por el virus en sí”, dice Michael Matthay, MD, profesor de medicina de la UCSF que ha estudiado enfermedades respiratorias agudas durante más de 30 años. Inevitablemente, un virus que se replica rápidamente matará o dañará muchas de las células pulmonares que infecta; cuantas más células infecte, más ruina dejará a su paso.
Pero el SARS-CoV-2 no parece ser un destructor salvaje de células. Aunque es demasiado pronto para saberlo con certeza, la tasa de mortalidad del virus parece ser aproximadamente 10 veces mayor que la de la gripe. “Uno pensaría que se debe a que es sólo una máquina de matar”, dice Max Krummel, PhD, Profesor de Patología Experimental de la UCSF y presidente de la iniciativa Bakar ImmunoX. Hasta ahora, sin embargo, la ciencia sugiere lo contrario.

“Una de las cosas más extrañas de este nuevo coronavirus es que no parece ser increíblemente citopático, con lo que nos referimos a matar células”, dice Krummel. “La gripe es realmente citopática; si se agrega a las células humanas en una placa de Petri, las células explotan en 18 horas”. Pero cuando los investigadores de la UCSF sometieron las células humanas al SARS-CoV-2, muchas de las células infectadas nunca perecieron. “Son datos bastante convincentes de que tal vez no estamos tratando con un virus muy agresivo”, dice Krummel.
Sospecha que la mayor provocación puede ser tu propio sistema inmunitario. Como cualquier patógeno, el SARS-CoV-2 desencadenará un ataque inmune a los pocos minutos de ingresar a tu cuerpo. Este contraataque es extraordinariamente complejo e involucra muchas tácticas, células y moléculas. En un estudio de la UCSF llamado COMET (COVID-19 Multi-Phenotyping for Effective Therapies), Krummel y otros científicos han estado observando esta guerra inmunitaria en más de 30 personas ingresadas en hospitales de UCSF con COVID-19 y otras infecciones respiratorias. “Lo que estamos haciendo es observar la sangre de los pacientes, sus genes y las secreciones de sus narices y pulmones, y nos preguntamos:” ¿Cuál es su ejército? ¿Cuál es su estrategia de respuesta? “
“Son datos bastante convincentes de que tal vez no estamos tratando con un virus muy agresivo”.
Krummel dice que un análisis temprano de los datos de COMET sugiere que los sistemas inmunes de muchos pacientes hospitalizados se movilizan de manera diferente y más agresiva contra el SARS-CoV-2 que contra los virus de la influenza, que causan la gripe. Sus pulmones están devastados, sugieren estos datos, no sólo por el virus sino por los detritos de una batalla inmunológica que salió mal. Esta respuesta inmune no autorizada podría explicar por qué, alrededor del día 11 de una infección por COVID-19, los pacientes a menudo desarrollan una neumonía grave conocida como síndrome de dificultad respiratoria aguda o SDRA.
En última instancia, COMET busca encontrar terapias COVID-19 que puedan controlar un sistema inmunitario demasiado ansioso para prevenir o tratar el SDRA. Pero esa hazaña no será fácil, dice Carolyn Calfee, MD, MAS ’09, experta en SDRA, profesora de medicina de la UCSF y co-líder del estudio. Explica que un tipo de intervención excesivo o incorrecto podría paralizar el sistema inmunitario de una persona hasta el punto de que no pueda eliminar una infección. “Es una línea muy fina entre terapéutica y efecto perjudicial”, dice Calfee. “Estamos tratando de encontrar ese equilibrio”.
Por lo general, las personas que mueren por SDRA derivada del COVID-19 mueren alrededor del día 19. Las tasas de mortalidad reportadas han variado ampliamente, siendo las tasas más altas donde la pandemia ha afectado a los recursos y al personal del hospital de forma más abrumadora. En los hospitales de la UCSF, probablemente debido a las órdenes tempranas de aislarse que se dieron en la ciudad y que impidieron un aumento inicial de los casos de COVID-19, hasta ahora sólo 10 de 85 pacientes críticos han muerto.
“La buena noticia es que hemos estado haciendo ensayos clínicos de las mejores prácticas de atención para el SDRA desde 1998”, dice Matthay. Gracias a la investigación realizada por él y otros, por ejemplo, los médicos han sabido durante mucho tiempo qué ajustes del ventilador provocan la menor cantidad de muertes y cómo voltear a los pacientes sobre sus estómagos, una técnica conocida como pronación, para ayudarlos a respirar mejor. Si las medidas de salud pública pueden mantener bajos los ingresos hospitalarios para que los proveedores de primera línea puedan hacer un buen uso de las habilidades y el conocimiento que ya tienen, es posible que tengamos menos que temer del SARS-CoV-2 de lo que pensábamos.
Por otro lado, el virus se comporta de maneras que aún son misteriosas.
Insuficiencia cardiaca
En abril, Susan Parson, MD, un médico forense del Área de la Bahía, hizo un descubrimiento sorprendente. Durante casi dos meses, las autoridades creyeron que las primeras personas en los EE. UU. que murieron por COVID-19 habían muerto de insuficiencia respiratoria en el estado de Washington a fines de febrero. En ese momento, los Centros para el Control y la Prevención de Enfermedades de EE. UU. limitaron las pruebas a las personas que tenían síntomas respiratorios y que habían viajado recientemente a China o habían estado expuestas al virus. Esas restricciones, sin embargo, resultaron ser equivocadas.
Como médico forense del condado de Santa Clara de California, Parson había realizado una autopsia de rutina a una mujer de 57 años llamada Patricia Dowd, quien murió repentinamente en su casa el 6 de febrero. En los tejidos de Dowd, Parson encontró la causa de su muerte: SARS-CoV-2. Pero el virus no había destrozado los pulmones de Dowd. De hecho, ella sólo tenía neumonía leve. En cambio, el SARS-CoV-2 le había roto el corazón.
Mientras tanto, los epidemiólogos comenzaron a descubrir que las enfermedades cardíacas preexistentes y las afecciones relacionadas ponen a las personas en mayor riesgo de sufrir y morir de COVID-19. “Estamos descubriendo que muchos pacientes que tienen formas más graves de la enfermedad son obesos, son diabéticos, hipertensos”, dice la cardióloga Nisha Parikh, MD, profesora asociada de la UCSF que se especializa en investigación de salud de la población. Dichos factores de riesgo, dice ella, son inusuales. “No son los que realmente se destacaron en epidemias anteriores”.
Los médicos también estaban viendo un sorprendente número de pacientes con COVID-19 que desarrollaban problemas cardíacos: debilidad muscular, inflamación, arritmias e incluso ataques cardíacos. “No estamos acostumbrados a que los virus respiratorios tengan consecuencias tan graves en el corazón en números aparentemente tan altos”, dice el cardiólogo Gregory Marcus, MD, MAS ’08, profesor de investigación de fibrilación auricular de la UCSF. Muchos pacientes cuyos corazones manifestaron estos síntomas también tenían pulmones dañados. Pero otros no tenían otros síntomas o, como Dowd, sólo síntomas leves.
Desde marzo, Marcus ha codirigido una de las encuestas comunitarias más grandes para comprender mejor la propagación del SARS-CoV-2 y sus innumerables efectos. El estudio, denominado Ciencia Ciudadana COVID-19, hasta ahora ha inscrito a más de 27,000 personas; cualquier persona con un teléfono inteligente puede participar. Marcus también planea comenzar a recopilar datos de dispositivos portátiles, incluidos los parches Fitbits y Zio, que monitorean de forma inalámbrica los ritmos cardíacos. “Puede haber un gran número de personas que sufren los efectos cardiovasculares del COVID-19 en ausencia de otros síntomas”, dice Marcus. “Me preocupa que nos perdamos esos casos”.
Es lógico que el SARS-CoV-2 afecte al corazón. Después de todo, las células cardíacas están al tope de receptores ACE2, el puerto vital de entrada del virus. Y, de hecho, los experimentos de laboratorio sugieren que el virus puede ingresar y replicarse en células cardíacas humanas cultivadas, dice Bruce Conklin, MD, profesor de medicina y experto en genética de enfermedades cardíacas en la UCSF y los Institutos Gladstone.
Pero Conklin no cree que el SARS-CoV-2 necesariamente mate las células cardíacas directamente. Más bien, en el proceso de copiarse a sí mismo, el virus roba partes de las instrucciones genéticas que le dicen a las células del corazón cómo hacer su trabajo. “Está arrastrando y secuestrando cosas que son necesarias para que el corazón lata”, dice. Actualmente está probando esta hipótesis utilizando células cardíacas humanas cultivadas en recipientes del tamaño de una copa en el laboratorio de Todd McDevitt, PhD, un bioingeniero de la UCSF y los Institutos Gladstone.
Sin embargo, también es posible que el sistema inmunitario de una persona infectada pueda causar la mayor parte del daño en el corazón, como parece hacer en los pulmones. “El corazón probablemente se infecta por muchos otros virus, y no tienen un efecto letal”, dice Conklin. “¿Qué hace que este sea diferente?”
Cosas extrañas
A fines de marzo, cuando San Francisco comenzó a calentarse, Sonia desarrolló pies fríos. Se puso calcetines de lana y aumentó la temperatura del calentador. Aún así, sus pies se sentían congelados. Tres días después, sus plantas se volvieron de color púrpura manchado.
Aparecieron puntos rojos en los dedos de sus pies. Por la noche, sus pies fríos picaban y quemaban. Caminar dolía. Y estaba exhausta, durmiendo la siesta durante las reuniones de Zoom vespertinas. “Fue muy extraño”, dice Sonia, residente de San Francisco. Una semana después, sus síntomas habían desaparecido.
“Sí, COVID”, escribió Lindy Fox, MD, profesora de dermatología de la UCSF, respondiendo a un correo electrónico que describe el caso de Sonia. Sonia no estaba sorprendida. Cualquiera, como ella, que haya estado siguiendo las noticias de la pandemia, probablemente haya oído hablar del “COVID en los dedos de los pies”, una erupción cutánea dolorosa o con picazón que a veces aparece en adultos jóvenes con casos de COVID-19 por lo demás leves o asintomáticos. “Se parece a lo que llamamos pernio, o sabañones”, dice Fox, “que es un fenómeno bastante común cuando alguien sale en clima frío: comienzan a tener protuberancias moradas o rosadas en los dedos de las manos o pies”.
Fox dice que muchas personas con erupciones cutáneas como la de Sonia no dan positivo para COVID-19, lo que ha hecho que algunos médicos se muestren escépticos sobre la conexión; cuando los pacientes tienen ambos, creen que es sólo una coincidencia. Pero Fox no lo cree así. Por un lado, “la época del año está mal”, dice ella. “El pernio suele aparecer en pleno invierno”. Aún más convincente, los dermatólogos de todo el mundo están “recibiendo un número enorme de llamadas al respecto”, dice Fox. “En las últimas tres semanas, he tenido entre 10 y 12 pacientes. Normalmente, tengo cuatro al año “.
Y no sólo los dermatólogos están agregando sus observaciones a la lista de síntomas en constante expansión del COVID-19. Los especialistas intestinales están descubriendo que del 20% al 40% de las personas con la enfermedad experimentan diarrea, náuseas o vómitos antes de otros síntomas, dice el gastroenterólogo Michael Kattah, MD, PhD, profesor asistente de la UCSF. Si tragas partículas de virus, dice, hay una buena probabilidad de que infecten las células que recubren su estómago, intestino delgado o colon. Como en los pulmones y el corazón, estas células están repletas con portales vulnerables de ACE2.

Kattah dice que es especialmente desconcertante cuanto tiempo parece persistir el virus en el intestino. Señala que alrededor del 50% de los pacientes con COVID-19 tienen partículas de virus en sus heces, a menudo durante semanas después de que sus muestras de hisopos nasales dan negativo. Los estudios de laboratorio muestran que estas partículas a menudo todavía están vivas y pueden infectar células en una placa de Petri. Sin embargo, si la transmisión fecal ocurre entre personas es una pregunta abierta. Si la respuesta es sí, las personas que se están recuperando de COVID-19 pueden necesitar permanecer en cuarentena incluso después de sentirse bien, y el resto de nosotros deberá ser tan meticuloso con respecto a la higiene del baño como lo hemos sido con respecto al lavado de manos y el uso de cubrebocas.
Otros especialistas también están sonando la alarma. Los neurólogos se preocupan por los informes de pacientes de COVID-19 con dolores de cabeza, “bruma mental”, pérdida del sentido del olfato, mareos, delirio y, en casos raros, accidente cerebrovascular. Los nefrólogos se preocupan por el estrés y la insuficiencia renal. Los hepatólogos se preocupan por las lesiones hepáticas. Los oftalmólogos se preocupan por la conjuntivitis. Mientras tanto, los pediatras se preocupan por un síndrome inflamatorio peculiar relacionado con COVID que aparece en niños y adultos jóvenes.
Los investigadores aún están resolviendo las causas de esta constelación de efectos. Si tiene un síntoma particular, ¿es porque el virus está atacando sus células? ¿Porque su sistema inmunológico está exagerando? ¿O sólo porque estás muy enfermo? En cualquier enfermedad grave, por ejemplo, los riñones deben trabajar muy duro para filtrar los desechos y controlar los nutrientes y líquidos; si están sobrecargados, pueden comenzar a fallar. Del mismo modo, los problemas cognitivos pueden ser el resultado del aumento de las toxinas en la sangre debido a los riñones estresados o por la falta de oxígeno debido a la dificultad respiratoria. “Hay mucho humo”, dice Michael Wilson, MD ’07, MAS ’16, profesor distinguido de Rachleff en el Instituto Weill de Neurociencias de la UCSF. “Tenemos que averiguar de dónde viene el fuego”.
Recientemente, se ha especulado que algunos de los síntomas aparentemente dispares de COVID-19 pueden provenir de problemas en la sangre. Los coágulos de sangre, por ejemplo, están apareciendo en casos de COVID-19 con la frecuencia suficiente para que los médicos lo noten. “Hay algo único sobre el sistema de coagulación en estos pacientes”, dice la nefróloga Kathleen Liu, MD ’99, PhD ’97, MAS ’07, profesora de medicina de la UCSF. En el cuidado de pacientes con COVID-19 en máquinas de diálisis, se sorprendió al ver que los coágulos de sangre bloquean los tubos de diálisis más de lo habitual. Los tubos bloqueados con coágulos son comunes, dice ella, “pero esto es extremo”.
Esto puede deberse a que, como lo sugiere la creciente evidencia, el SARS-CoV-2 puede infectar células en las paredes de los vasos sanguíneos que ayudan a regular el flujo sanguíneo y la coagulación, o los coágulos. Si es cierto, este comportamiento podría explicar algunas de las manifestaciones más raras (y poco comunes) del virus, como ataques cardíacos, derrames cerebrales e incluso “COVID en los dedos de los pies”.
“Nuestra vasculatura es un sistema contiguo”, dice el cardiólogo Parikh. “Por lo tanto, las lesiones en un área, como los vasos sanguíneos en los pulmones, pueden desencadenar cascadas de coágulos que afectan a múltiples órganos”. Algunos de esos problemas probablemente se deben a la inflamación desencadenada por el sistema inmunitario, señala, aunque otro culpable puede ser el RAAS del cuerpo, o el sistema renina-angiotensina-aldosterona, un sistema hormonal que controla la presión arterial y el equilibrio de líquidos. Debido a que el RAAS involucra a los receptores ACE2, Parikh sospecha que se puede interrumpir cuando el virus infecta las células a través de estos receptores, lo que desencadena la coagulación y otros efectos posteriores. Su laboratorio ahora está estudiando este sistema en pacientes con COVID-19 para comprender mejor cómo lo afecta la infección por SARS-CoV-2.
Inevitablemente, algunas dolencias pueden llegar a ser pistas falsas. Durante una pandemia, cuando las personas acuden en masa a hospitales con infecciones, los médicos también verán un aumento en otros problemas de salud, simplemente por las reglas estadísticas, señala S. Andrew Josephson, MD, presidente de neurología del departamento de la UCSF, y miembro del Instituto Weill para Neurociencias. “Si la prevalencia de la infección es alta, entonces casi cualquier afección, una pierna rota, por así decirlo, podrías concluir que está asociada con COVID-19”.
“Como médicos clínicos, queremos llevar información a nuestra comunidad médica y al público lo más rápido posible”, dice Josephson, “pero debemos ser cautelosos para no hacer un gran problema de algo pequeño”.

La larga cola
Al igual que con cualquier infección, la duración de un episodio de COVID-19 varía de persona a persona. Si estás lo suficientemente enfermo como para necesitar cuidados críticos, puedes esperar que la enfermedad demore al menos unas semanas en seguir su curso. En algunos casos, los síntomas persisten durante meses. Sin embargo, para un caso típico más leve, deberías sentirte mejor en un par de semanas.
En ese punto, la pregunta más importante en tu mente será: ¿Soy inmune? Ahora hay más de una docena de pruebas de anticuerpos en el mercado, pero la mayoría no son confiables, según la investigación de la UCSF. E incluso las mejores pruebas no pueden decirte si tienes suficientes anticuerpos adecuados para protegerte contra la reinfección. “Hay muchas esperanzas y creencia de que nos haremos de una prueba de anticuerpos que en realidad nos informe de la inmunidad, pero todavía no estamos allí”, dice Chaz Langelier, MD, PhD, profesor asistente de medicina de la UCSF que está trabajando para mejorar las herramientas de diagnóstico para COVID-19.
Mientras tanto, tenemos muchas incógnitas: si te vuelves inmune al SARS-CoV-2, ¿cuándo y cómo ocurre? ¿Ganarás inmunidad por un caso leve o asintomático, así como por uno grave? ¿Cuánto durará esa inmunidad?
“Las respuestas tendrán enormes implicaciones para el distanciamiento social y el uso de cubrebocas y para que la economía vuelva a funcionar”, dice Michael Peluso, MD, un investigador clínico que vino a UCSF hace tres años para ayudar a combatir el VIH. Ahora está codirigiendo un nuevo estudio llamado LIINC (Impacto a largo plazo de la infección con el nuevo coronavirus), que está inscribiendo a personas que han sido infectadas con SARS-CoV-2 y las seguirá durante dos años. Además de traer luz a los cambios en la inmunidad con el paso del tiempo, LIINC está investigando los efectos crónicos de la infección en el sistema inmunitario, los pulmones, el corazón, el cerebro, la sangre y otras partes del cuerpo.
“Espero que las personas se recuperen y la inmunidad sea protectora y duradera, y eso será todo”, dice Peluso.
Es lo que todos esperamos. Esperamos vencer una infección rápidamente o, mejor aún, evitar el virus hasta que haya una vacuna. Esperamos que si caemos gravemente enfermos, seremos cuidados por los mejores proveedores y atendidos por personas que amamos. La realidad, como ya sabemos, es más complicada. E incluso si el COVID-19 no golpea nuestros cuerpos, la pandemia seguramente dejará cicatrices, en nuestras psiques, nuestros medios de vida, nuestras instituciones y nuestra salud, que apenas estamos comenzando a comprender. Ciertamente, no sabemos que suerte nos tocará, como individuos o como personas. Sólo el tiempo, y los datos, lo dirán.
Traducido de We Thought It Was Just a Respiratory Virus. We were wrong. Por Ariel Bleicher y Katherine Conrad para UCSF Magazine. Traducción: Armando Alvarez










2 comentarios
Excelente reportaje. Muy interesante, sorprendente y hasta preocupante.
Ilustra muchísimo para conocer lo que es el virus y lo que desencadena en el cuerpo humano. Vaya paquete al que nos enfrentamos.
Los felicito. Da gusto encontrar portales periodísticos como este. Saludos.
Es realmente desconsolador ver que despues de 7 meses de esta pesadilla por la que estamos pasando se sepa muy poco sobre la naturaleza, efectos y curación definitiva de este virus, pero confiamos en esas personas tan comprometidas que lo estan intentando, un aplauso para todos esos grandes médicos y científicos que están luchando por cada uno de nosotros, que Dios los ilumine para lograrlo y los llene de bendiciones-